Готовые домашние задания по химии к учебнику О. С. Габриелян "ХИМИЯ 8 класс"
Практическая работа № 7 (9).
«Условия протекания химических реакций между растворами электролитов до конца»
Опыт 1.
Выполнение работы:
Взяли 3 пробирки; в первую прилили растворы сульфата меди (II) и гидроксида натрия, наблюдаем выпадение голубого осадка:
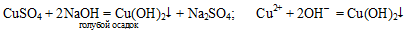
Во вторую пробирку прилили растворы хлорида калия и фосфата натрия. Ничего не происходит:
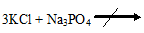 реакция не идет, т.к. не образуется газ, осадок или вода.
реакция не идет, т.к. не образуется газ, осадок или вода.
В третью пробирку прильем растворы сульфата алюминия и хлорида бария, наблюдаем выпадение белого осадка:
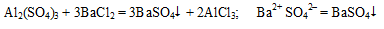
Вывод: реакции идут до конца, если одним из продуктов является осадок.
Опыт 2.
Выполнение работы:
В две пробирки налили раствор: сульфита натрия в первую и карбоната натрия во вторую и затем в каждую прилили раствор азотной кислоты, Наблюдаем выделение пузырьков газа:
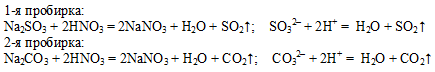
образуется белый творожистый осадок.
Опыт З
Выполнение работы:
а) В пробирку налили немного раствора гидроксида натрия и добавили несколько капель индикатора фенолфталеина. Раствор окрашивается в розовый цвет, так как среда щелочная. После приливания раствора соляной кислоты раствор обесцветился так как раствор вновь стал нейтральным.
NаОН + НСl = NaCl + Н2O; OН– + Н+ = Н2O
б) В пробирку налили примерно до половины раствора сульфата меди (II) и добавили немного раствора гидроксида натрия. Наблюдаем выпадение осадка голубого цвета. При приливании раствора серной кислоты осадок растворяется, так как происходит реакция нейтрализации:
CuSO4 +2NaOH = Cu(OH)2↓ + Na2SO4; Cu2+ + 2OH– = Cu(OH)2↓;
Cu(OH)2 + H2SO4 = CuSO2 + 2H2O; Cu(OH)2 + 2H+ = Cu2+ + 2H2O.
Вывод: Все основания вступают в реакцию нейтрализации.